LCHM1253
Devoir de cristallographie:
Ce devoir va porter sur l'analyse de la structure du MOF-801.
Qu'est-ce qu'un MOF ?
Un MOF est un solide poreux appelé réseau métallo-organique en français. C'est une structure constituée d'ions métalliques ou de clusters coordonnés à des ligands organiques. Leurs numéros sont souvent donnés selon leur lieu de découverte.
À travers ce devoir, dans un premier temps nous aborderons sa composition et ses caractéristiques. Par la suite ce devoir abordera sa structure cristalline, pour ensuite parler de ses propriétés et fonctions. Le dernier point de ce document sera les méthodes expérimentales que l'on peut utiliser afin d'analyser ce matériau.
1. Analyse cristallographique:
- Maille cristalline:
La structure cristallise dans le système cubique. Les paramètres de maille sont les suivants:
a = b = c = 17,8348 (17) Å
α = β = γ = 90°
Son volume est de: V = 5672.9(16) ų
Le nombre de formules par maille est de: Z = 4
L'égalité des paramètres de maille et angles droits correspondent à une maille cubique primitive.
- Système cristallin et réseau de Bravais:
Son système cristallin est cubique et le réseau de Bravais peut être cubique primitif (P) ou bien cubique à faces centrées (F) en fonction de l'arrangement des ligands.
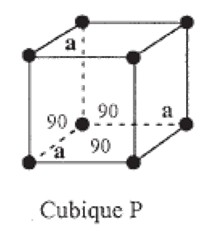
Comme illustré ci-dessus, la structure réelle (P) ne possède des nœud uniquement aux sommets, contrairement à la structure idéale (F) qui en a également au centre de ses faces.
- Groupe spatial:
La symétrie idéale du MOF-801 est souvent décrite selon le réseau Fm-3m (cubique à faces centrées). Cependant, en analysant le fichier CIF, on constate qu'il nous indique le groupe spatial Pn-3. Bien que non étudié au cours, cette symétrie est une version primitive du réseau dans laquelle les ligands fumarates réduisent légèrement la symétrie globale. Ce groupe spatial se caractérise par une haute symétrie présentée ci-dessous.
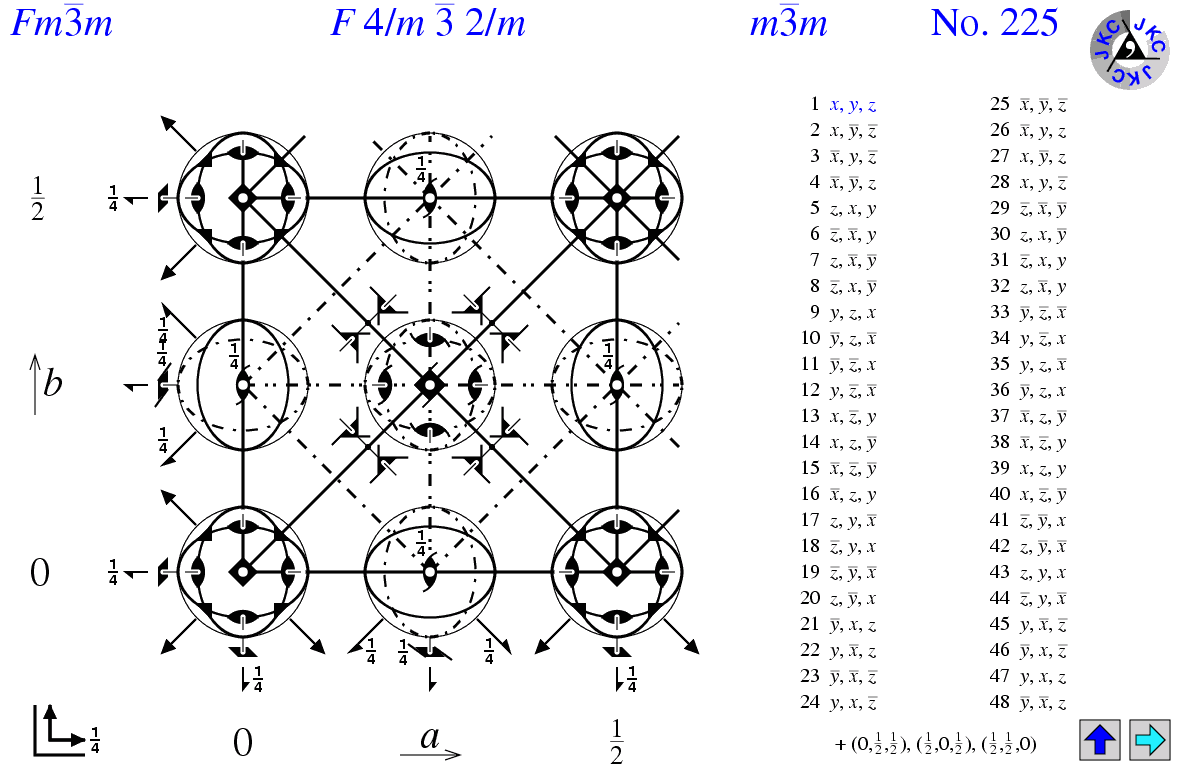
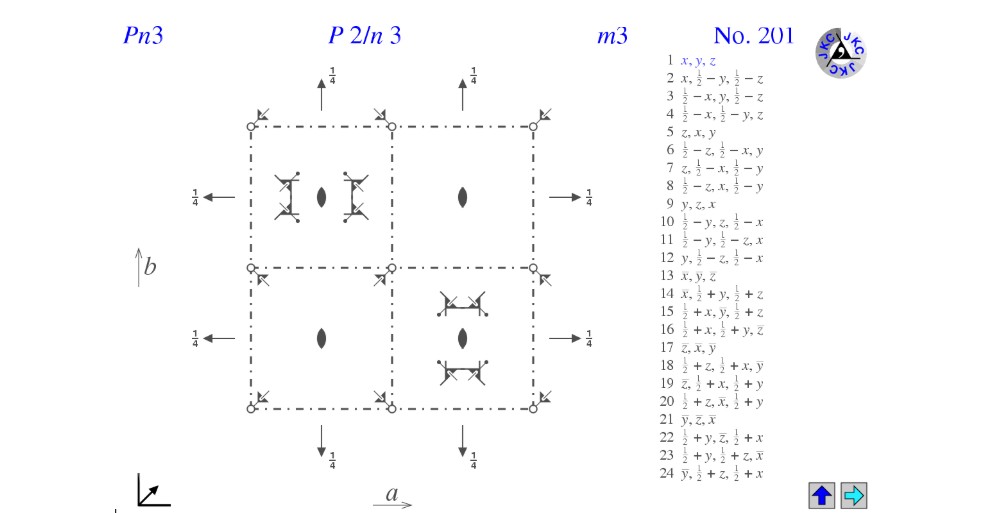
- Symétrie dans la maille:
La maille de mon matériau présente un centre d'inversion, elle contient également des axes de rotation d'ordre 3 le long des diagonales du cube. On y retrouve aussi des axes de rotation d'ordre 2 et des plans de glissement de type n.
- Contenu de la maille:
La formule réduite de mon matériau est la suivante: C₂₄H₁₂O₃₂Zr₆. En l'occurrence, avec Z = 4 la maille contient 24 atomes de zirconium,128 atomes d'oxygène,96 atomes de carbone et 48 atomes d'hydrogène.
2. Structure cristalline:
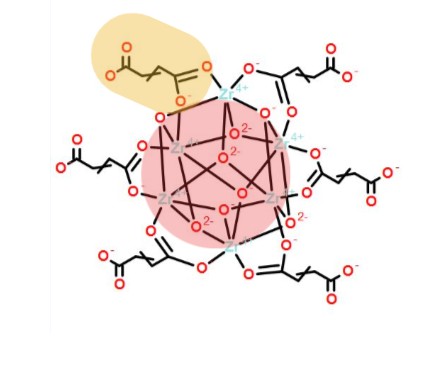
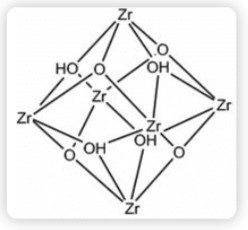
- Nœud inorganique ( cluster Zr₆O₄(OH)₄) :
Le nœud inorganique présent dans le MOF-801 (entouré en rouge) est le cluster Zr₆O₄(OH)₄, il contient 6 atomes de Zirconium disposés en géométrie octaédrique et reliés par des ponts oxo et hydroxo. Cela forme ensemble une unité compacte. Les atomes de zirconium sont arrangés selon une géométrie interne régulière. Chaque cluster possède des sites de coordination disposés autour de lui afin d'accueillir les ligands.
Ce cluster défini la connectivité et la topologie du matériau et sert de point d'ancrage multiple pour la fixation des ligands car il constitue l'unité inorganique du réseau.
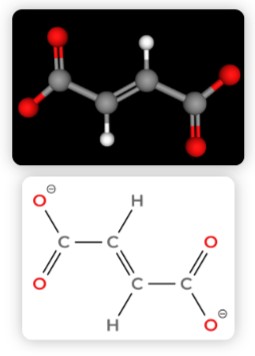
- Fumarate:
Le fumarate (entouré en orange) est un anion dérivé de l'acide fumarique dont la formule est la suivante : C₄H₂O₄²⁻. Cet anion contient une double liaison C=C en configuration trans avec un groupe carboxylate (-COO⁻) de chaque côté de cette dernière. Ces deux groupements donnent donc une géométrie allongée et relativement rigide. Cette rigidité permet d'éviter l'effondrement dans la maille lors de la déshydratation.
De plus, le fumarate est bidenté car chaque carboxylate a la capacité d'agir comme site donneur d'électrons. Lui permettant de se lier simultanément à deux centres métalliques.
D'un point de vue moléculaire, c'est une petite molécule organique favorisant la formation de ponts réguliers entre nœuds inorganiques dans les MOF.
3. Propriétés et fonctions:
- Fonctions du MOF-801:
Le MOF-801 présente plusieurs fonctions parmi lesquelles on retrouve notamment : capturer et stocker des molécules grâce à son réseau poreux régulier. Il est également utilisé afin d'adsorber et séparer des gaz grâce au remplissage d'espace (spacefilling) et à la topologie du réseau.
Il peut également agir comme matrice de stockage pour de petites molécules ( tel que l'eau). Ce réseau métal-organique à base de zirconium présente une affinité forte quant à l'adsorption d'eau, avec une capacité d'environ 0,21 à 0,24g d'eau par gramme de matériau.
Sa structure ordonnée lui sert de support pour certaines réactions hétérogènes ou bien pour des dispositifs de libération contrôlée. En outre, le MOF-801 agit comme support de coordination.
- Propriétés :
Le MOF-801 est un matériau poreux cristallin 3D ( groupe d'espace Fm3̅m) à maille cubique présentant une grande surface interne et une porosité bien définie. Cette porosité est le résultat de l'organisation périodique des clusters métalliques et des ligands organiques, offrant au MOF une connectivité tridimensionnelle répétitive.
Les pores de mon MOF sont hydrophiles, cela grâce à la présence de groupements hydroxyles et des sites métalliques polaires. Ils favorisent l'adsorption de molécules d'eau par le biais d'interactions type liaisons hydrogène. Mon matériau se distingue également par une stabilité thermique plutôt élevée ( environ jusqu'à 300°C) et une grande résistance à l'hydrolyse.
Sa structure est périodique et il n'existe pas sous forme d'entités isolées, mais bien comme un réseau cristallin étendu.
4. Méthodes expérimentales :
Afin de comprendre comment on passe d'un cristal de MOF-801 à un signal mesurable, on utilise des outils mathématiques de la cristallographie :
Conditions de diffraction : afin d'obtenir un signal, le réseau réciproque du MOF doit entrer en contact avec la sphère d'Ewald. Cette construction géométrique de rayon 1/λ illustre la condition physique où les ondes diffusées par les atomes de Zr et de C interfèrent de manière constructive. Ainsi, un pic de diffraction apparait lorsqu'un nœud du réseau réciproque se trouve exactement sur la surface de cette sphère.
- La diffraction à rayons x (DRX) :
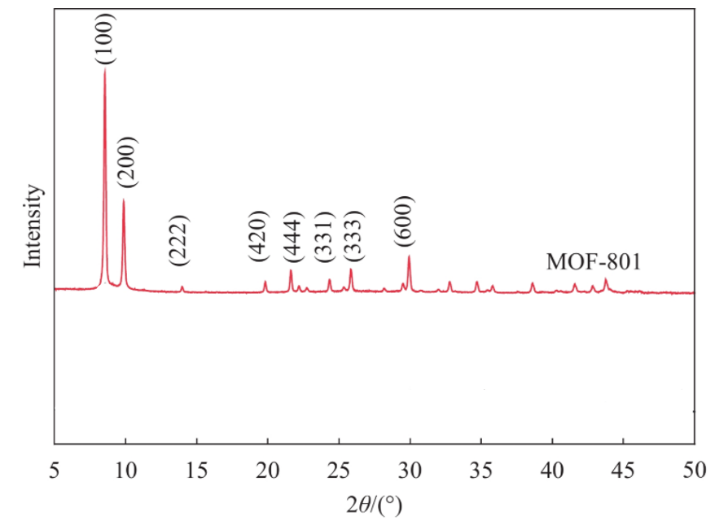
Cette méthode permet de passer de la structure décrite du MOF dans l'espace réel par sa maille aux informations dans l'espace réciproque. Ainsi, chaque point du réseau réciproque correspond à une famille de plans atomiques (désignés hkl) de l'espace direct. La diffraction des rayons X sur poudre (DRX) permet de vérifier la structure interne du MOF-801 et constitue la preuve structurelle de la réussite de sa synthèse.
Dans ce diffractogramme, chaque pic d'intensité correspond à une interaction spécifique entre le faisceau de rayons X et l'organisation périodique des atomes dans le cristal. Les pics nets et leur correspondance avec le modèle théorique indiquent que le matériau est cristallin car au plus le signal est fin, au plus le domaine de cohérence cristalline est grand et ordonné. Le pic principal vers 8,5° est caractéristique de son réseau. Étant donné sa disposition à petit angle, on peut en conclure qu'une grande distance inter-réticulaire est présente grâce à la loi de Bragg stipulant qu'au plus l'angle de diffraction est petit, plus la distance entre les plans d'atomes est grande.
Voici la loi de Bragg:
(preuve mathématique que si l'angle téta est petit, alors d est grand)
- La spectroscopie infrarouge à transformation de Fourier (FTIR) :
La spectroscopie infrarouge à transformation de Fourier est une technique d'analyse permettant d'identifier la nature des liaisons chimies dans un matériau. Cette dernière repose sur la mesure de l'absorption d'énergie par les molécules. Ce qui provoque ainsi des vibrations spécifiques qui s'expriment toutes différemment en fonction de chaque groupe fonctionnel.
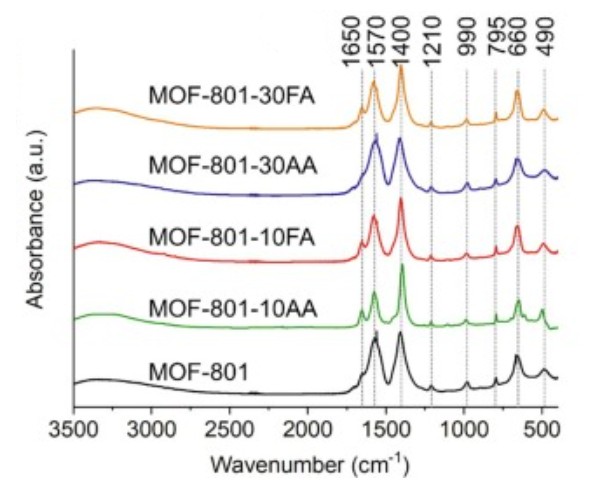
Sur ce spectre présent ci-contre, les bandes intenses situées à 1650 et 1570 cm⁻¹ témoignent qu'un ligand organique fumarate est bien présent et correspond aux vibrations d'élongation des groupements carboxylates.
Ensuite, les signaux situés entre 990 et 490 cm⁻¹ nous traduisent les modes de vibration des liaisons métal-oxygène (Zr-O). Cela témoigne de la coordination directe entre les clusters de Zr et les ligands organiques. Ces informations valident ainsi la formation d'un réseau poreux et la pureté chimique du composé.
En identifiant précisément les interactions moléculaires présentes, la FTIR garantit le bon assemblage chimique du MOF-801.
FAQ
1. Pourquoi ne voit-on pas bien l'hydrogène en rayons x ?
Car le facteur de diffusion f dépend du nombre d'électrons Z présents dans l'atome. L'hydrogène n'a qu'un électron, il est donc presque invisible par rapport au Zirconium qui en a 40.
2. Pourquoi le Zirconium est-il la star de mon diffractogramme ?
Parce que selon la diffusion de Thomson, ce sont les électrons qui diffractent. Avec 40 électrons (Z=40), le Zr a un facteur de structure dominant par rapport au Carbone (Z=6) des ligands.
3. Pourquoi ai-je choisis cette structure ?
J'ai été très intriguée lorsque nous avons visité les laboratoires de Monsieur Filinchuk et que son assistant nous a parlé des MOFs, ces petits matériaux qui sont capables d'adsorber des petites molécules et qui ont une structure particulièrement complexe. Au départ, cette structure je la trouvais compliquée car elle ne parait pas simple à première vue. Après avoir approfondi mes recherches, j'ai été convaincue de choisir cette structure car elle est très impressionnante et possède des propriétés très intéressantes.